Молекулярные методы диагностики новой коронавирусной инфекции: сравнение петлевой изотермической амплификации и полимеразной цепной реакции
- Авторы: Акимкин В.Г.1, Петров В.В.1, Красовитов К.В.1, Борисова Н.И.1, Котов И.А.1, Родионова Е.Н.1, Черкашина А.С.1, Кондрашева Л.Ю.1, Тиванова Е.В.1, Хафизов К.Ф.1
-
Учреждения:
- ФБУН «Центральный научно-исследовательский институт эпидемиологии» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (Роспотребнадзор)
- Выпуск: Том 66, № 6 (2021)
- Страницы: 417-424
- Раздел: ОРИГИНАЛЬНЫЕ ИССЛЕДОВАНИЯ
- URL: https://journal-vniispk.ru/0507-4088/article/view/118199
- DOI: https://doi.org/10.36233/0507-4088-86
- ID: 118199
Цитировать
Аннотация
Введение. В настоящее время основой молекулярной диагностики большинства инфекционных заболеваний является использование полимеразной цепной реакции с обратной транскрипцией (ОТ-ПЦР; reverse transcription polymerase chain reaction, RT-PCR). Альтернативой этому методу при решении диагностических задач могут выступать технологии, основанные на петлевой изотермической амплификации с обратной транскрипцией (ОТИТ; reverse transcription loop-mediated isothermal amplifcation, RT-LAMP). В данном исследовании нами выполнено сравнение ОТ-ИТ и ОТ-ПЦР с целью анализа как преимуществ, так и недостатков обоих подходов.
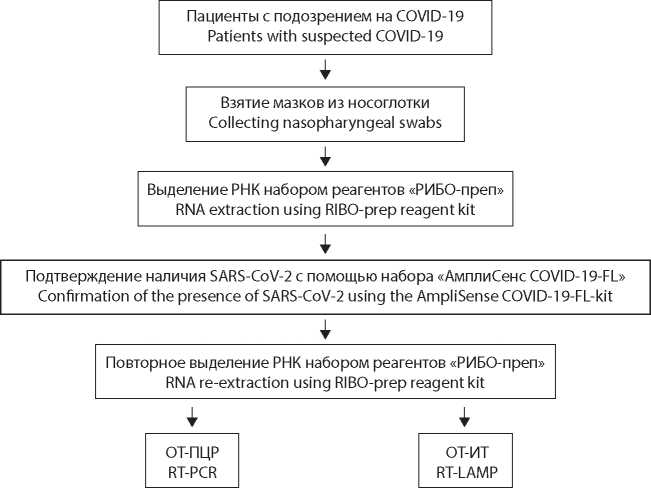
Материал и методы. При проведении экспериментов использованы наборы реагентов, предназначенные для анализа на основе ОТ-ПЦР и ОТ-ИТ. В работе использовался биологический материал, полученный из мазков со слизистой оболочки рото- и носоглотки у лиц с симптомами новой коронавирусной инфекции.
Результаты. В ходе исследования протестирован 381 образец РНК вируса SARS-CoV-2 (Coronaviridae: Coronavirinae: Betacoronavirus; Sarbecovirus) от различных пациентов. Полученные значения порогового числа циклов (cycle threshold, Ct) для ОТ-ПЦР составили в среднем 20,0 ± 3,7 (диапазон 1530 ± 300 с), для ОТ-ИТ – 12,8 ± 3,7 (диапазон 550 ± 160 с). Исходя из теоретических предпосылок, в качестве гипотетической была предложена линейная зависимость представленных величин; коэффициент корреляции составил ≈0,827. При этом для проб с низкой вирусной нагрузкой (ВН) более высокие значения Ct при ОТ-ИТ не всегда соответствовали таковым в случае ОТ-ПЦР.
Обсуждение. Мы отметили существенное преимущество во времени при выполнении анализа с помощью ОТ-ИТ по сравнению с ОТ-ПЦР, что может быть важно в условиях тестирования большого количества образцов. Разработанные на основе методики ОТ-ИТ тест-системы в силу простоты в использовании и относительной быстроты получения результата могут быть применены в процессе массового скрининга с целью выявления лиц со средней и высокой ВН, представляющих наибольшую угрозу распространения SARS-CoV-2. В свою очередь, диагностические методы на базе ОТ-ПЦР подходят в том числе для оценки ВН и её динамики у пациентов c COVID-19.
Полный текст
Открыть статью на сайте журналаОб авторах
В. Г. Акимкин
ФБУН «Центральный научно-исследовательский институт эпидемиологии» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (Роспотребнадзор)
Email: fake@neicon.ru
ORCID iD: 0000-0003-4228-9044
111123, Москва, Россия
РоссияВ. В. Петров
ФБУН «Центральный научно-исследовательский институт эпидемиологии» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (Роспотребнадзор)
Email: fake@neicon.ru
ORCID iD: 0000-0002-3503-2366
111123, Москва, Россия
РоссияК. В. Красовитов
ФБУН «Центральный научно-исследовательский институт эпидемиологии» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (Роспотребнадзор)
Email: fake@neicon.ru
ORCID iD: 0000-0001-7237-1810
111123, Москва, Россия
РоссияН. И. Борисова
ФБУН «Центральный научно-исследовательский институт эпидемиологии» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (Роспотребнадзор)
Email: fake@neicon.ru
ORCID iD: 0000-0002-9672-0648
111123, Москва, Россия
РоссияИ. А. Котов
ФБУН «Центральный научно-исследовательский институт эпидемиологии» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (Роспотребнадзор)
Email: fake@neicon.ru
ORCID iD: 0000-0003-2416-5689
111123, Москва, Россия
РоссияЕ. Н. Родионова
ФБУН «Центральный научно-исследовательский институт эпидемиологии» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (Роспотребнадзор)
Email: fake@neicon.ru
ORCID iD: 0000-0003-0192-1832
111123, Москва, Россия
РоссияА. С. Черкашина
ФБУН «Центральный научно-исследовательский институт эпидемиологии» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (Роспотребнадзор)
Email: fake@neicon.ru
ORCID iD: 0000-0002-1888-4903
111123, Москва, Россия
РоссияЛ. Ю. Кондрашева
ФБУН «Центральный научно-исследовательский институт эпидемиологии» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (Роспотребнадзор)
Email: fake@neicon.ru
ORCID iD: 0000-0002-0147-4262
111123, Москва, Россия
РоссияЕ. В. Тиванова
ФБУН «Центральный научно-исследовательский институт эпидемиологии» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (Роспотребнадзор)
Email: fake@neicon.ru
ORCID iD: 0000-0003-1286-2612
111123, Москва, Россия
РоссияК. Ф. Хафизов
ФБУН «Центральный научно-исследовательский институт эпидемиологии» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (Роспотребнадзор)
Автор, ответственный за переписку.
Email: kkhafizov@gmail.com
ORCID iD: 0000-0001-5524-0296
Хафизов Камиль Фаридович, канд. биол. наук, руководитель научной группы разработки новых методов диагностики на основе технологий секвенирования следующего поколения отдела молекулярной диагностики и эпидемиологии
111123, Москва, Россия
РоссияСписок литературы
- Wu Z., McGoogan J.M. Characteristics of and important lessons from the coronavirus disease 2019 (COVID-19) outbreak in China: summary of a report of 72 314 cases from the Chinese Center for Disease Control and Prevention. JAMA. 2020; 323(13): 1239–42. https://doi.org/10.1001/jama.2020.2648
- Sharfstein J.M., Becker S.J., Mello M.M. Diagnostic Testing for the Novel Coronavirus. JAMA. 2020; 323(15): 1437–8. https://doi.org/10.1001/jama.2020.3864
- Drosten C., Göttig S., Schilling S., Asper M., Panning M., Schmitz H., et al. Rapid detection and quantification of RNA of Ebola and Marburg viruses, Lassa virus, Crimean-Congo hemorrhagic fever virus, Rift Valley fever virus, dengue virus, and yellow fever virus by real-time reverse transcription-PCR. J. Clin. Microbiol. 2002; 40(4): 2323–30. https://doi.org/10.1128/jcm.40.7.2323-2330.2002
- Mackay I.M., Arden K.E., Nitsche A. Real-time PCR in virology. Nucleic Acids Res. 2002; 30(6): 1292–305. https://doi.org/10.1093/nar/30.6.1292
- Tahamtan A., Ardebili A. Real-time RT-PCR in COVID-19 detection: issues affecting the results. Expert Rev. Mol. Diagn. 2020; 20(5): 453–4. https://doi.org/10.1080/14737159.2020.1757437
- Lu R., Wu X., Wan Z., Li Y., Zuo L., Qin J., et al. Development of a novel reverse transcription loop-mediated isothermal amplification method for rapid detection of SARS-CoV-2. Virol. Sin. 2020; 35(3):344–7. https://doi.org/10.1007/s12250-020-00218-1
- Jiang M., Pan W., Arasthfer A., Fang W., Ling L., Fang H., et al. Development and validation of a rapid, single-step reverse transcriptase loop-mediated isothermal amplification (RT-LAMP) system potentially to be used for reliable and high-throughput screening of COVID-19. Front. Cell Infect. Microbiol. 2020; 10: 331. https://doi.org/10.3389/fcimb.2020.00331
- Notomi T., Okayama H., Masubuchi H., Yonekawa T., Watanabe K., Amino N., et al. Loop-mediated isothermal amplification of DNA. Nucleic Acids Res. 2000; 28(12): E63. https://doi.org/10.1093/nar/28.12.e63
- Хафизов К.Ф., Петров В.В., Красовитов К.В., Золкина М.В., Акимкин В.Г. Экспресс-диагностика новой коронавирусной инфекции с помощью реакции петлевой изотермической амплификации. Вопросы вирусологии. 2021; 66(1): 17–28. https://doi.org/10.36233/0507-4088-42
- Parida M., Posadas G., Inoue S., Hasebe F., Morita K. Real-time reverse transcription loop-mediated isothermal amplification for rapid detection of West Nile virus. J. Clin. Microbiol. 2004; 42(1):257–63. https://doi.org/10.1128/jcm.42.1.257-263.2004
- Zhao Y., Chen F., Li Q., Wang L., Fan C. Isothermal amplification of nucleic acids. Chem. Rev. 2015; 115(22): 12491–545. https://doi.org/10.1021/acs.chemrev.5b00428
- Bruno A., de Mora D., Freire-Paspuel B., Rodriguez A.S., Paredes- Espinosa M.B., Olmedo M., et al. Analytical and clinical evaluation of a heat shock SARS-CoV-2 detection method without RNA extraction for N and E genes RT-qPCR. Int. J. Infect. Dis. 2021; 109: 315–20. https://doi.org/10.1016/j.ijid.2021.06.038
- Lalli M.A., Langmade J.S., Chen X., Fronick C.C., Sawyer C.S., Burcea L.C., et al. Rapid and Extraction-Free Detection of SARS-CoV-2 from Saliva by Colorimetric Reverse-Transcription Loop-Mediated Isothermal Amplification. Clin. Chem. 2021; 67(2):415–24. https://doi.org/10.1093/clinchem/hvaa267
- Anastasiou O.E., Holtkamp C., Schäfer M., Schön F., Eis-Hübinger A.M., Krumbholz A. Fast Detection of SARS-CoV-2 RNA Directly from Respiratory Samples Using a Loop-Mediated Isothermal Amplification (LAMP) Test. Viruses. 2021; 13. https://doi.org/10.3390/v13050801
- Thompson D., Lei Y. Mini review: Recent progress in RT-LAMP enabled COVID-19 detection. Sensors and Actuators Reports. 2020; 2: 100017. http://dx.doi.org/10.1016/j.snr.2020.100017
- Borisova N.I., Kotov I.A., Kolesnikov A.A., Kaptelova V.V., Speranskaya A.S., Kondrasheva L.Yu., et al. Monitoring the spread of the SARS-CoV-2 (Coronaviridae: Coronavirinae: Betacoronavirus; Sarbecovirus) variants in the Moscow region using targeted high-throughput sequencing. Voprosy Virusologii. 2021; 66(4):269–78. https://doi.org/10.36233/0507-4088-72
- Cevik M., Tate M., Lloyd O., Maraolo A.E., Schafers J., Ho A. SARS-CoV-2, SARS-CoV, and MERS-CoV viral load dynamics, duration of viral shedding, and infectiousness: a systematic review and meta-analysis. Lancet Microbe. 2021; 2(1): e13–22. https://doi.org/10.1016/s2666-5247(20)30172-5
- Zhou F., Yu T., Du R., Fan G., Liu Y., Liu Z., et al. Clinical course and risk factors for mortality of adult inpatients with COVID-19 in Wuhan, China: a retrospective cohort study. Lancet. 2020; 395(10229):1054–62. https://doi.org/10.1016/s0140-6736(20)30566-3
- La Scola B., Le Bideau M., Andreani J., Hoang V.T., Grimaldier C., Colson P., et al. Viral RNA load as determined by cell culture as a management tool for discharge of SARS-CoV-2 patients from infectious disease wards. Eur. J. Clin. Microbiol. Infect. Dis. 2020; 39(6): 1059–61. https://doi.org/10.1007/s10096-020-03913-9
- Bullard J., Dust K., Funk D., Strong J.E., Alexander D., Garnett L., et al. Predicting infectious severe acute respiratory syndrome coronavirus 2 from diagnostic samples. Clin. Infect. Dis. 2020; 71(10):2663–6. https://doi.org/10.1093/cid/ciaa638
- Mora-Cárdenas E., Marcello A. Switch-on the LAMP to spot Zika. Ann. Transl. Med. 2017; 5(24): 500. https://doi.org/10.21037/atm.2017.10.19
- Augustine R., Hasan A., Das S., Ahmed R., Mori Y., Notomi T., et al. Loop-mediated isothermal amplification (LAMP): A rapid, sensitive, specific, and cost-effective point-of-care test for coronaviruses in the context of COVID-19 pandemic. Biology (Basel). 2020; 9(8): 182. https://doi.org/10.3390/biology9080182
- Rabe B.A., Cepko C. SARS-CoV-2 detection using isothermal amplification and a rapid, inexpensive protocol for sample inactivation and purification. Proc. Natl. Acad. Sci. USA. 2020; 117(39):24450–8. https://doi.org/10.1073/pnas.2011221117
- Yu L., Wu S., Hao X., Dong X., Mao L., Pelechano V., et al. Rapid detection of COVID-19 coronavirus using a reverse transcriptional loop-mediated isothermal amplification (RT-LAMP) diagnostic platform. Clin. Chem. 2020; 66(7): 975–7. https://doi.org/10.1093/clinchem/hvaa102
Дополнительные файлы