Clinical characteristics of newborn with different birth weight (results of a multicenter cohort study)
- Authors: Deev I.A1, Kulikova K.V1, Kobyakova O.S1, Kulikov E.S1, Holopov A.V2, Stepanov I.A3, Antonova I.N4, Bybchenko E.G3, Holtzman K.E5, Dorovskaja E.N6, Kozhevnikova E.N3, Ledyakina L.V7, Makarova N.A6, Permyakova M.A4, Popova N.G6, Stradina A.A7, Fedorova L.A8, Fomenko A.A5, Kharitonova E.S5, Khodosevich E.B5, Chugainova I.N4
-
Affiliations:
- Siberian State Medical University, Ministry of Healthcare of the Russian Federation
- Tomsk Region Health Department
- Regional Perinatal Center
- Perm Regional Clinical Hospital
- St Nicholas Children’s Municipal Hospital No 17
- Trans-Baikal Regional Perinatal Center
- Mordovia Republican Clinical Perinatal Center
- St Petersburg State Pediatric Medical University, Ministry of Healthcare of the Russian Federation
- Issue: Vol 7, No 4 (2016)
- Pages: 67-76
- Section: Articles
- URL: https://journal-vniispk.ru/pediatr/article/view/5970
- DOI: https://doi.org/10.17816/PED7467-76
- ID: 5970
Cite item
Full Text
Abstract
Full Text
Введение
Благодаря созданию на территории Российской Федерации (РФ) перинатальных центров, оказывающих высокотехнологичную и специализированную помощь и обеспечивающих внедрение современных технологий в области выхаживания детей с массой тела при рождении менее 2500 г и сроком гестации менее 37 недель, выживаемость таких новорожденных имеет тенденцию к увеличению [1, 3, 4, 8].
Согласно данным отечественных и зарубежных авторов, число недоношенных детей в настоящее время составляет порядка 20 % [1, 5, 7]. При этом по мере снижения неонатальной смертности маловесных новорожденных все большее влияние на прогноз жизни и здоровья таких детей в будущем оказывают состояния, ассоциированные с недоношенностью: бронхолегочная дисплазия (БЛД), некротический энтероколит (НЭК), внутрижелудочковые кровоизлияния (ВЖК), ретинопатия, нарушения слуха, транзиторный гипотиреоз и др. [2, 4, 6, 8–10].
В этой связи интересным представляется анализ клинической характеристики детей с различной массой тела, что явилось одной из целей спланированного и проведенного нами многоцентрового, когортного исследования новорожденных.
Материалы и методы
В исследовании, проведенном по единому протоколу, приняли участие 5 перинатальных центров: г. Томск, г. Саранск, г. Пермь, г. Чита, г. Санкт-Петербург (включение исследовательских центров в настоящий момент открыто для всех желающих, набор пациентов продолжается, подробная информация представлена на сайте ФГБОУ ВО «Сибирский государственный медицинский университет» Министерства здравоохранения Российской Федерации http://www.ssmu.ru/ru/nauka/projekts/npkin/). Во всех центрах в исследование были включены дети, рожденные живыми, вне зависимости от срока гестации и массы тела при рождении, а также при условии подписания информированного согласия со стороны родителей и/или законных представителей ребенка. Критериями исключения являлись нежелание родителей и/или законных опекунов пациента принимать участие в исследовании на любом из этапов, а также несоответствие пациента критериям включения.
В рамках протокола был предусмотрен визит включения пациента на момент рождения (Визит 0), на котором происходила регистрация следующих данных: антропометрические показатели (масса и длина тела, окружность груди и живота), путь родоразрешения, оценка по шкале Апгар, необходимость проведения дополнительной оксигенации и/или респираторной поддержки в 36 недель постконцептуального возраста или 56 суток жизни (в зависимости от срока гестации при рождении), данные первичного инструментального обследования (ультразвуковое исследование головного мозга, внутренних органов, аудиологический скрининг) и заключения врачей-специалистов; ретроспективный сбор анамнестических данных об отце и матери в течение 6 месяцев до момента наступления беременности и в течение всего периода вынашивания ребенка (Визит –1), а также визит проспективного наблюдения детей в возрасте 12 месяцев (Визит 1) (рис. 1).
В результате изучения анамнестических данных матери установлено, что отдельно взятые характеристики биологического и социального анамнеза женщины (возраст, масса тела, рост, хроническая сопутствующая патология, курение во время беременности, отсутствие высшего образования, незамужний статус и т. д.) достоверно сопряжены с вероятностью рождения ребенка с массой тела менее 2500 г. Так, например, изолированный показатель массы тела женщины при постановке на учет в женскую консультацию менее 75 кг ассоциирован с 6-кратным увеличением шанса рождения маловесного новорожденного (ОШ = 5,79; ДИ 95 % 3,5–9,4), вместе с тем сочетание таких факторов, как возраст матери старше 35 лет, рост менее 165 см и анемия во время беременности, взаимосвязано с 12-кратным увеличением вероятности рождения ребенка с массой тела менее 2500 г (ОШ = 12,18; ДИ 95 % 1,6–93,9) в сравнении с женщинами, не имевшими данных факторов риска. Комплекс других характеристик матери: масса тела при постановке на учет в женскую консультацию менее 75 кг и рост менее 165 см, а также наличие хронических заболеваний, вне зависимости от локализации, ассоциированы с 14-кратным увеличением шанса рождения маловесного пациента (ОШ = 14,40; ДИ 95 % 2,9–70,5).
Данная статья посвящена анализу клинической характеристики пациентов, включенных в многоцентровое когортное исследование, на момент рождения (Визит 0) (см. рис. 1).
Для статистической обработки данных использован пакет программ Statistica for Windows version 10.0, а также программа Statcalc version 6 с целью расчета отношения шансов (ОШ) и доверительного интервала 95 % (ДИ 95 %). При сравнении частот качественных признаков использовался критерий χ2, или 2-сторонний критерий Фишера. Для оценки различия средних в попарно не связанных выборках применяли U-критерий Манна – Уитни, в связанных — критерий Вилкоксона. Качественные данные представлены в виде абсолютных или относительных (%) частот, количественные — в виде Х ± х, где Х — среднее арифметическое, х — стандартное отклонение. Разницу значений считали значимой при p < 0,05.
Результаты
В исследовании проанализированы данные 572 детей (351 мальчик, 221 девочка), которые были распределены в зависимости от массы тела при рождении: 83 ребенка с нормальной массой тела (группа 1), 188 детей с низкой массой тела (группа 2), 179 пациентов с очень низкой массой тела (группа 3) и 122 новорожденных с экстремально низкой массой тела (группа 4) (см. рис. 1).

Рис. 1. Схема исследования: *Норм. МТ — нормальная масса тела; НМТ — низкая масса тела; ОНМТ — очень низкая масса тела; ЭНМТ — экстремально низкая масса тела
Анализ антропометрических параметров при рождении детей, включенных в исследование, показал, что наименьшие показатели зарегистрированы в группе с экстремально низкой массой тела (табл. 1).
Таблица 1. Характеристика антропометрических показателей пациентов, включенных в исследование, в зависимости от группы по массе тела при рождении
Антропометрические | Дети, включенные в исследование n = 572 | |||
Норм. МТ^ n = 83 | НМТ^ n = 188 | ОНМТ^ n = 179 | ЭНМТ^ n = 122 | |
Масса, г | 3333,11 ± 258,98 | 1941,67 ± 280,26 | 1319,16 ± 142,19 | 812,21 ± 139,59* |
Рост, см | 51,89 ± 1,78 | 44,21 ± 2,58 | 39,11 ± 2,36 | 33,93 ± 3,21* |
Окружность головы, см | 32,64 ± 1,02 | 30,64 ± 1,51 | 27,59 ± 1,52 | 24,19 ± 1,79* |
Окружность груди, см | 32,43 ± 1,05 | 28,14 ± 1,71 | 24,93 ± 1,52 | 21,69 ± 1,76* |
Примечание: *р < 0,05 при сравнении антропометрических показателей в группе 4 в сравнении с другими группами (U-test Mann-Whitney); ^Норм. МТ — масса тела; ^НМТ — низкая масса тела; ^ОНМТ — очень низкая масса тела; ^ЭНМТ — экстремально низкая масса тела | ||||
Характеристика методов родоразрешения продемонстрировала, что во всей изучаемой популяции преобладающим способом было кесарево сечение (62,41 vs 37,59 %), р < 0,05. Стратификация пациентов, включенных в исследование, в зависимости от массы тела при рождении показала, что в группе с нормальной массой тела достоверно преобладало естественное рождение (91,57 vs 8,43 %), в то время как дети с НМТ, ОНМТ ЭНМТ чаще рождались с использованием метода оперативного родоразрешения (р < 0,05) (рис. 2). При этом установлено, что в изучаемой выборке снижение массы тела при рождении менее 2500 г ассоциировано с увеличением вероятности оперативного способа рождения более чем в 27 раз (ОШ = 27,33; ДИ 95 % 12,3–60,8) в сравнении с детьми, имевшими нормальную массу тела на момент Визита 0.
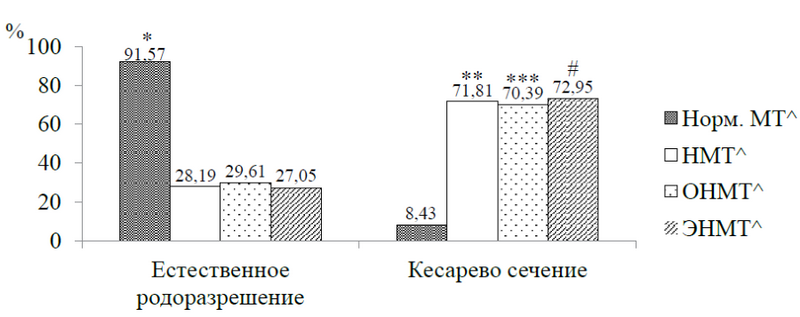
Рис. 2. Характеристика пациентов, включенных в исследование, в зависимости от группы по массе тела при рождении и методов родоразрешения: *р < 0,05 при сравнении детей в группе нормальной массы тела в зависимости от способа родоразрешения; **р < 0,05 при сравнении пациентов в группе НМТ в зависимости от способа родоразрешения; ***р < 0,05 при сравнении пациентов в группе ОНМТ в зависимости от способа родоразрешения; # р < 0,05 при сравнении пациентов в группе ЭНМТ в зависимости от способа родоразрешения; ^Норм. МТ — масса тела; ^НМТ — низкая масса тела; ^ОНМТ — очень низкая масса тела; ^ЭНМТ — экстремально низкая масса тела
Оценка по шкале Апгар у пациентов в исследуемой популяции показала, что на 1-й минуте среднее количество баллов достоверно различалось во всех группах, при этом статистически наименьшее число было зарегистрировано в выборке детей с экстремально низкой массой тела при рождении (5,24 ± 1,65 балла; р < 0,05) (рис. 3). В последующем наблюдении к 5-й минуте отмечался достоверный рост количества баллов во всех группах пациентов вне зависимости от массы тела при рождении, однако, несмотря на положительную динамику показателя, исследуемый параметр в выборке ЭНМТ был значимо ниже, при этом достоверные различия установлены во всех группах в сравнении с детьми, имевшими нормальную массу тела (см. рис. 3).
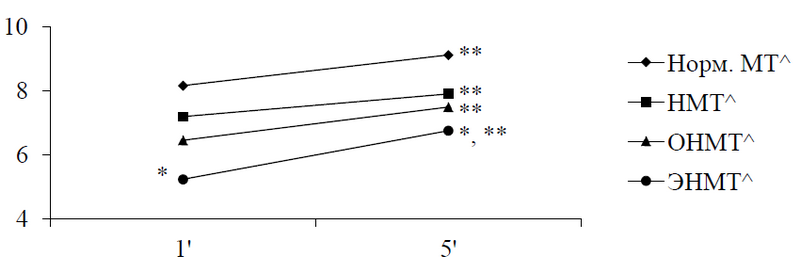
Рис. 3. Результаты оценки по шкале Апгар на 1-й и 5-й минутах в зависимости от группы по массе тела при рождении: * p < 0,05 при сравнении показателя среднего балла по шкале Апгар между группами по массе тела (U-test Mann-Whitney); ** p < 0,05 при сравнении показателя среднего балла по шкале Апгар на 1-й и 5-й минутах (test Wilcoxon); ^Норм. МТ — масса тела; ^НМТ — низкая масса тела; ^ОНМТ — очень низкая масса тела; ^ЭНМТ — экстремально низкая масса тела
Корреляционный анализ показал наличие прямой статистической зависимости между массой тела при рождении и оценками по шкале Апгар на 1-й (r = 0,70; р < 0,05) и 5-й минутах (r = 0,64; р < 0,05).
В структуре сопутствующих состояний у детей, включенных в исследование, было установлено, что в группе нормальной массы тела доля новорожденных, имевших какую-либо патологию, составила 5,26 %, в то время как в выборке детей с массой тела при рождении менее 2500 г данный показатель был равен 94,74 % (р < 0,05). Вероятность наличия заболеваний в неонатальном периоде (описанных в рамках данной работы) у новорожденных в группах НМТ, ОНМТ, ЭНМТ была в 25 раз выше (ОШ = 25,05; ДИ 95 % 13,3–47,4) в сравнении с детьми, имевшими нормальную массу тела на момент Визита 0.
Ретинопатия недоношенных в изучаемой популяции новорожденных достоверно чаще регистрировалась в группе ЭНМТ в сравнении с детьми, имевшими ОНМТ при рождении (63,93 vs 18,99 %; р < 0,05), при этом также было установлено статистически достоверное различие показателя среднего срока гестации у пациентов в группах ОНМТ (28,94 ± 1,37 недели) и ЭНМТ (26,15 ± 1,46 недели), имевших данное заболевание (р < 0,05). Вероятность формирования ретинопатии недоношенных у пациентов с массой тела менее 1000 г была в 7 раз выше (ОШ = 7,56; ДИ 95 % 4,5–12,8) в сравнении с новорожденными, имевшими очень низкую массу тела при рождении.
Геморрагическое поражение центральной нервной системы (ЦНС) I степени среди новорожденных, включенных в исследование, наиболее часто фиксировалось в группе ОНМТ в сравнении с группами НМТ и ЭНМТ (17,88 %; р < 0,05). Перинатальное поражение ЦНС (ПП ЦНС) гипоксически-ишемического генеза и развитие судорожного синдрома в неонатальном периоде в изучаемой популяции регистрировались только у пациентов с массой тела при рождении менее 2500 г, при этом частота была сопоставима между группами (табл. 2). Вероятность формирования геморрагического поражения ЦНС I степени в исследуемой популяции была в 2 раза выше у новорожденных с массой тела при рождении менее 1500 г (ОШ = 2,47; ДИ 95 % 1,3–4,6) в сравнении с детьми с низкой массой тела при рождении. Взаимосвязи между шансом возникновения внутрижелудочковых кровоизлияний II, III, VI степеней и группами пациентов, включенных в исследование, установлено не было, важно, что ЭНМТ при рождении в исследуемой популяции была ассоциирована с 3-кратным повышением вероятности развития судорожного синдрома в неонатальном периоде (ОШ = 3,11; ДИ 95 % 1,1–8,5) в сравнении с детьми, имевшими низкую массу тела при рождении.
Таблица 2. Структура сопутствующих состояний у детей, включенных в исследование, в зависимости от группы по массе тела при рождении
Сопутствующие состояния | Дети, включенные в исследование n = 572 | |||
Норм. МТ^ n (%) | НМТ^ n (%) | ОНМТ^ n (%) | ЭНМТ^ n (%) | |
Без сопутствующих состояний | 65 (78,31)* | 109 (57,98)* | 52 (29,05) | 4 (3,28)*** |
Ретинопатия недоношенных | 0 | 0 | 34 (18,99) | 78 (63,93)& |
Ангиопатия сосудов сетчатки | 12 (14,46) | 6 (3,19) | 0 | 2 (1,64) |
Врожденные аномалии развития | 0 | 8 (4,26) | 6 (3,35) | 6 (4,92) |
Перинатальное поражение центральной нервной системы гипоксически-ишемического генеза | 0 | 6 (3,19) | 8 (4,47) | 2 (1,64) |
Судорожный синдром | 0 | 10 (5,32) | 6 (3,35) | 12 (9,84) |
ВЖК I степени | 0 | 14 (7,45) | 32 (17,88) ^^ | 18 (14,75) |
ВЖК II степени | 0 | 6 (3,19) | 2 (1,12) | 0 |
ВЖК III степени | 0 | 0 | 0 | 10 (8,20) |
ВЖК IV степени | 0 | 0 | 0 | 2 (1,64) |
Открытый артериальный проток | 0 | 30 (15,96) ^^^ | 70 (39,11) | 79 (64,75) |
Транзиторный гипотиреоз | 0 | 10 (5,32)# | 102 (56,98) ** | 114 (93,44) ** |
Бронхолегочная дисплазия | 0 | 5 (2,66) | 20 (11,17) | 53 (43,44) ## |
Некротический энтероколит | 0 | 0 | 4 (2,23) | 8 (6,56) |
Примечание: * р < 0,05 при сравнении пациентов в группах без сопутствующих состояний в сравнении с теми, кому были диагностированы патологические заболевания; ** р < 0,05 при сравнении пациентов в группах по массе тела, имевших транзиторный гипотиреоз, в сравнении с другими патологическими заболеваниями; *** р < 0,05 при сравнении пациентов в группах по массе тела, не имевших сопутствующих состояний; & р < 0,05 при сравнении пациентов в группах по массе тела, имевших ретинопатию недоношенных; ^^ р < 0,05 при сравнении пациентов в группах по массе тела, имевших ВЖК I степени; ^^^р < 0,05 при сравнении пациентов в группах по массе тела, имевших открытый артериальный проток; # р < 0,05 при сравнении пациентов в группах по массе тела, имевших транзиторный гипотиреоз; ## р < 0,05 при сравнении пациентов в группах по массе тела, имевших бронхолегочную дисплазию; ^Норм. МТ — масса тела; ^НМТ — низкая масса тела; ^ОНМТ — очень низкая масса тела; ^ЭНМТ — экстремально низкая масса тела | ||||
Открытый артериальный проток и транзиторный гипотиреоз в изучаемой выборке детей достоверно реже встречались в группе пациентов, имевших НМТ при рождении, в сравнении с пациентами в выборках ОНМТ и ЭНМТ (р < 0,05) (табл. 2). Масса тела менее 1500 г в изучаемой популяции была ассоциирована с 5-кратным увеличением шанса персистирования открытого артериального протока (ОШ = 5,17; ДИ 95 % 3,3–8,1) и 45-кратным увеличением вероятности развития транзиторного гипотиреоза (ОШ = 45,23; ДИ 95 % 22,8–89,7) в сравнении с детьми, имевшими низкую массу тела на момент Визита 0.
Бронхолегочная дисплазия в 36 недель постконцептуального возраста статистически чаще диагностировалась у пациентов с массой тела при рождении менее 1000 г в сравнении с группами НМТ и ОНМТ (43,44 %; р < 0,05) (см. табл. 2). Вероятность формирования БЛД в изучаемой популяции у детей с массой тела при рождении от 1500 до 1000 г была выше в 5 раз (ОШ = 4,60; ДИ 95 % 1,7–12,5) в сравнении с группой детей, имевших НМТ, в то время как экстремально низкая масса тела при рождении была ассоциирована с 28-кратным шансом развития изучаемого заболевания (ОШ = 28,11; ДИ 95 % 10,8–73,3) в сравнении с новорожденными, имевшими низкую массу тела на момент Визита 0.
Результат анализа данных аудиологического скрининга новорожденных, включенных в исследование, показал, что отсутствие незарегистрированной отоакустической эмиссии (ОАЭ) достоверно чаще фиксировалось в группе ЭНМТ вне зависимости от стороны наблюдения (правое и левое ухо) (рис. 4). При этом вероятность получения незарегистрированной ОАЭ с правой стороны в изучаемой популяции была в 7 раз выше у детей, имевших массу тела при рождении от 1500 до 1000 г и менее 1000 г, в сравнении с детьми с низкой массой тела на момент Визита 0 (ОШ = 6,85; ДИ 95 % 2,4–19,5 и ОШ = 7,86; ДИ 95 % 3,9–15,5 соответственно). С другой стороны, анализ данных аудиологического скрининга левого уха показал 22-кратное повышение шанса отсутствия регистрации ОАЭ в изучаемой выборке в группе пациентов с ОНМТ (ОШ = 21,82; ДИ 95 % 5,3–90,5) и 15-кратное повышение — в случае рождения ребенка с ЭНМТ (ОШ = 14,93; ДИ 95 % 7,8–28,6) в сравнении с новорожденными, имевшими массу тела при рождении от 1500 до 2500 г.
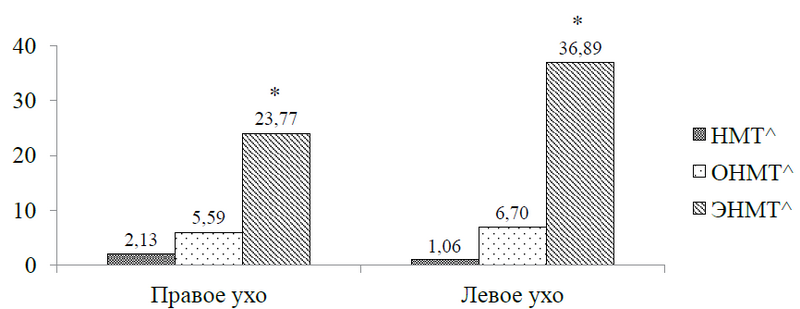
Рис. 4. Результаты аудиологического скрининга у детей, включенных в исследование, в зависимости от группы по массе тела при рождении и отсутствия регистрации отоакустической эмиссии: * р < 0,05 при сравнении пациентов в группе ЭНМТ, не имевших зарегистрированную отоакустическую эмиссию, в сравнении с другими группами; ^НМТ — низкая масса тела; ^ОНМТ — очень низкая масса тела; ^ЭНМТ — экстремально низкая масса тела
Обсуждение
Таким образом, проведенный анализ клинической характеристики пациентов, включенных в исследование, с различной массой тела при рождении показал, что увеличение частоты оперативного родоразрешения и снижение количества баллов по шкале Апгар, а также ряд патологических состояний в наибольшей степени характерны для детей, имевших массу тела при рождении менее 1500 г, что в большинстве случаев корреспондирует с данными когортных исследований новорожденных, проведенных другими авторами [2, 4, 6].
Структура патологических состояний, описанных в рамках данной работы, представлена преимущественно ретинопатией недоношенных, геморрагическим поражением ЦНС, судорожным синдромом в неонатальном периоде, транзиторным гипотиреозом, бронхолегочной дисплазией, некротическим энтероколитом, гемодинамически значимыми нарушениями сердечно-сосудистой системы, а также отсутствием регистрации ОАЭ при проведении аудиологического скрининга с последующим формированием тугоухости различного генеза.
Дети, включенные в исследование, с нормальной массой тела на момент Визита 0 в структуре изучаемых патологических состояний в неонатальном периоде имели только ангиопатию сосудов сетчатки в 14,46 % случаев, при этом других сопутствующих нозологических форм установлено не было. Учитывая тот факт, что результаты проведенного нами анализа показали наибольшую вероятность возникновения изучаемых патологических состояний в группах детей с массой тела при рождении менее 1500 г (ОНМТ и ЭНМТ), было проведено исследование вероятности наличия сочетания 3 и более заболеваний (описанных в рамках данной работы) со стратификацией когорты пациентов, включенных в исследование, по признаку массы тела при рождении: до 1000 г и от 1000 до 1500 г. Анализ отношения шансов показал, что в случае, когда масса тела при рождении менее 1000 г, вероятность наличия трех и более описанных заболеваний у ребенка выше в 44 раза (ОШ = 44,52; ДИ 95 % 15,5–127,5), в то время как при достижении новорожденным очень низкой массы тела при рождении (1000–1500 г) шансы развития трех и более патологических состояний были достоверно выше только в 7 раз (ОШ = 7,12; ДИ 95 % 2,4–20,9) в сравнении с детьми, имевшими низкую массу тела.
Таким образом, в настоящее время существует необходимость не только использования современных технологий выхаживания маловесных новорожденных, но и обеспечения превентивной помощи в группе женщин с высокой степенью перинатального риска с возможностью выявления различных факторов-предикторов рождения пациентов с массой тела менее 2500 г у матери (возраст, масса тела, рост, хроническая сопутствующая патология, курение во время беременности, отсутствие высшего образования, незамужний статус и т. д.), что, в свою очередь, может способствовать предупреждению преждевременных родов или пролонгированию беременности до 32 недель и/или массы тела плода свыше 1000 г и, как следствие, улучшению показателей выживаемости недоношенных пациентов [2, 3].
Финансирование. Исследование не имело спонсорской поддержки.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
About the authors
Ivan A Deev
Siberian State Medical University, Ministry of Healthcare of the Russian Federation
Author for correspondence.
Email: ivandeyev@yandex.ru
MD, PhD, Dr Med Sci, Professor, Department of Faculty Pediatrics Russian Federation
Kristina V Kulikova
Siberian State Medical University, Ministry of Healthcare of the Russian Federation
Email: kristina.v.kulikova@gmail.com
Assistant Professor Russian Federation
Olga S Kobyakova
Siberian State Medical University, Ministry of Healthcare of the Russian Federation
Email: olga_kobyakova@rambler.ru
MD, PhD, Dr Med Sci, Professor, Head, Department of General Medical Practice Russian Federation
Evgeny S Kulikov
Siberian State Medical University, Ministry of Healthcare of the Russian Federation
Email: evgeny.s.kulikov@gmail.com
MD, PhD, Dr Med Sci, Associate Professor, Department of General Medical Practice Russian Federation
Aleksandr V Holopov
Tomsk Region Health Department
Email: alexholopov@rambler.ru
MD, PhD, Head of Department Russian Federation
Igor A Stepanov
Regional Perinatal Center
Email: stepanovOPC@mail.ru
MD, PhD, Deputy of Chief of Perinatal Centre Russian Federation
Irina N Antonova
Perm Regional Clinical Hospital
Email: irina123a@mail.ru
Pediatrician, Department of Follow-up and Rehabilitation Treatment of Young Children Russian Federation
Elena G Bybchenko
Regional Perinatal Center
Email: elena.1982.ru@mail.ru
MD, PhD, Neonatologist, Department of Neonatal Pathology Russian Federation
Kirill E Holtzman
St Nicholas Children’s Municipal Hospital No 17
Email: kg_fox@hotmail.com
Neurologist, 2nd Department Russian Federation
Elena N Dorovskaja
Trans-Baikal Regional Perinatal Center
Email: el.dorovskay@yandex.ru
Deputy of Chief for Pediatric Care Russian Federation
Ekaterina N Kozhevnikova
Regional Perinatal Center
Email: kozhevnikova.en@yandex.ru
Pediatrician, Department of Follow-up of Clinical-Diagnostic Department Russian Federation
Ludmila V Ledyakina
Mordovia Republican Clinical Perinatal Center
Email: kristina.v.kulikova@gmail.com
MD, PhD, Dr Med Sci, Deputy of Chief for Pediatric Care Russian Federation
Natalia A Makarova
Trans-Baikal Regional Perinatal Center
Email: makarova-nat@yandex.ru
Head, Department of Neonatal Intensive Care Russian Federation
Maria A Permyakova
Perm Regional Clinical Hospital
Email: masha.permiakova@yandex.ru
Pediatrician, Department of Follow-up and Rehabilitation Treatment of Young Children Russian Federation
Nadezhda G Popova
Trans-Baikal Regional Perinatal Center
Email: popovaneo@mail.ru
MD, PhD, Associate Professor, Department of Pediatrics FPC PPP Russian Federation
Anna A Stradina
Mordovia Republican Clinical Perinatal Center
Email: gofj@mail.ru
Neonatologist, Department of Neonatal and Premature Infants Russian Federation
Larisa A Fedorova
St Petersburg State Pediatric Medical University, Ministry of Healthcare of the Russian Federation
Email: arslarissa@rambler.ru
MD, PhD Russian Federation
Anna A Fomenko
St Nicholas Children’s Municipal Hospital No 17
Email: gvozdik1985@mail.ru
Neurologist, 2nd Department Russian Federation
Ekaterina S Kharitonova
St Nicholas Children’s Municipal Hospital No 17
Email: romanovaes@mail.ru
Neurologist, 2nd Department Russian Federation
Ekaterina B Khodosevich
St Nicholas Children’s Municipal Hospital No 17
Email: katerina_laru@mail.ru
Neurologist, 2nd Department Russian Federation
Irina N Chugainova
Perm Regional Clinical Hospital
Email: ira.ch09@mail.ru
Head, Department of Follow-up and Rehabilitation Treatment of Young Children Russian Federation
References
- Антонов А.Г., Борисевич О.А., Буркова А.С., и др. Интенсивная терапия и принципы выхаживания детей с экстремально низкой и очень низкой массой тела при рождении / Под ред. Е.Н. Байбариной, Д.Н. Дегтярева, В.И. Широковой. Методическое письмо. – М., 2012. – С. 5. [Antonov АG, Borisevich ОА, Burkova АS, et al. Intensive therapy and principles of nursing of children with extremely low and very low birth weight. Ed by Е.N. Baibarina, D.N. Degtyarev, V.I. Shirokova. Metodicheskoe pismo. Moscow; 2012. P. 5. (In Russ.)]
- Деев И. А., Куликова К.В., Деева Е.В., и др. Клиническая характеристика детей с очень низкой и экстремально низкой массой тела при рождении // Российский педиатрический журнал. – 2016. – Т. 19. – № 4. – С. 209–216. [Deev IA, Kulikova KV, Deeva EV. Clinical characteristics of children with very low and extremely low birth weight. Rossijskij pediatricheskij zhurnal. 2016;19(4):209-216. (In Russ.)]
- Деев И. А., Куликова К.В., Куликов Е.С., и др. Анализ факторов риска рождения ребенка с очень низкой и экстремально низкой массой тела при рождении // Мать и дитя в Кузбассе. – 2016. – № 2. – С. 10–15. [Deev IA, Kulikova KV, Kulikov ES, et al. Analysis of risk factors for having children with very low and extremely low birth weight. Mat’ i Ditja v Kuzbasse. 2016;(2):10-15. (In Russ.)]
- Логвинова И.И., Емельянова А.С. Факторы риска рождения маловесных детей, структура заболеваемости, смертности // Российский педиатрический журнал. – 2000. – № 3. – С. 50–52. [Logvinova II, Emeljanova АS. Risk factors of low birth weight children, structure of morbidity, mortality. Rossijskij pediatricheskij zhurnal. 2000;(3):50-52. (In Russ.)]
- Beck S, Wojdyla D, Say L, et al. The worldwide incidence of preterm birth: a systematic review of maternal mortality and morbidity. Bull World Health Organ. 2010 Jan; 88(1):31-8. doi: 10.2471/BLT.08.062554. Epub 2009 Sep 25.
- Cheong JL, Doyle LW. Increasing rates of prematurity and epidemiology of late preterm birth. Paediatr. Child Health. 2012;48(9):784-8. doi: 10.1111/j.1440-1754.
- 02536.x.
- Howson CP, Kinney MV, McDougall L, Lawn JE. Born too soon: preterm birth matters. Reprod Health. 2013;10(Suppl 1: S1). doi: 10.1186/1742-4755-10-S1-S1. Epub 2013 Nov 15.
- Majnemer A, Riley P, Shevell M, et al. Severe bronchopulmonary dysplasia increases risk for later neurological and motor sequelae in preterm survivors. Dev Med Child Neurol. 2000;42(1):53-60. doi: 10.1111/j.1469-8749.2000.tb00025.x.
- Schieve LA, Tian LH, Rankin K, et al. Population impact of preterm birth and low birth weight on developmental disabilities in US children. Ann Epidemiol. 2016.Apr;26(4):267-74. doi: 10.1016/j.ann¬epidem.2016.02.012. Epub 2016 Mar 22.
- Soll RF. Progress in the Care of Extremely Preterm Infant. JAMA. 2015.Sep. 8; 314(10):1007-8. doi: 10.1001/jama.2015.10911.
Supplementary files







