Популяционный иммунитет к SARS-CoV-2 населения Новосибирской области на фоне пандемии COVID-19
- Авторы: Попова А.Ю.1, Смирнов В.С.2, Ежлова Е.Б.1, Мельникова А.А.1, Самойлова Л.В.3, Лялина Л.В.2, Семёнова Е.В.4, Гурский М.А.4, Аксёнова Е.А.5, Арбузова Т.В.2, Тотолян А.А.2
-
Учреждения:
- Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека (Роспотребнадзор)
- ФБУН «Санкт-Петербургский научно-исследовательский институт эпидемиологии и микробиологии им. Пастера» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (Роспотребнадзор)
- Управление Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (Роспотребнадзор) по Новосибирской области
- ФБУЗ «Центр гигиены и эпидемиологии в Новосибирской области»
- Министерство здравоохранения Новосибирской области
- Выпуск: Том 66, № 4 (2021)
- Страницы: 299-309
- Раздел: ОРИГИНАЛЬНЫЕ ИССЛЕДОВАНИЯ
- URL: https://journal-vniispk.ru/0507-4088/article/view/118193
- DOI: https://doi.org/10.36233/0507-4088-54
- ID: 118193
Цитировать
Полный текст
Аннотация
Цель. Определить уровень серопревалентности SARS-CoV-2 среди населения Новосибирской области на фоне пандемии COVID-19.
Материалы и методы. Работу проводили в 2 фазы: 1) поперечное когортное исследование выполняли с 28.06. по 15.07.2020 г.; 2) продольный когортный 3-этапный серомониторинг: 1-й этап 28.06–15.07.2020 г., 2-й – 14.09–04.10.2020 г., 3-й – 10–30.12.2020 г. Работу проводили по единой методике, разработанной Роспотребнадзором при участии НИИЭМ им. Пастера с учетом рекомендаций ВОЗ. Содержание антител IgG к нуклеокапсиду SARS-CoV-2 определяли методом ИФА с использованием набора реагентов производства ГНЦПМиБ (г. Оболенск) по инструкции производителя. Статистический анализ проводили с помощью Microsoft Excel 2010 и других программ.
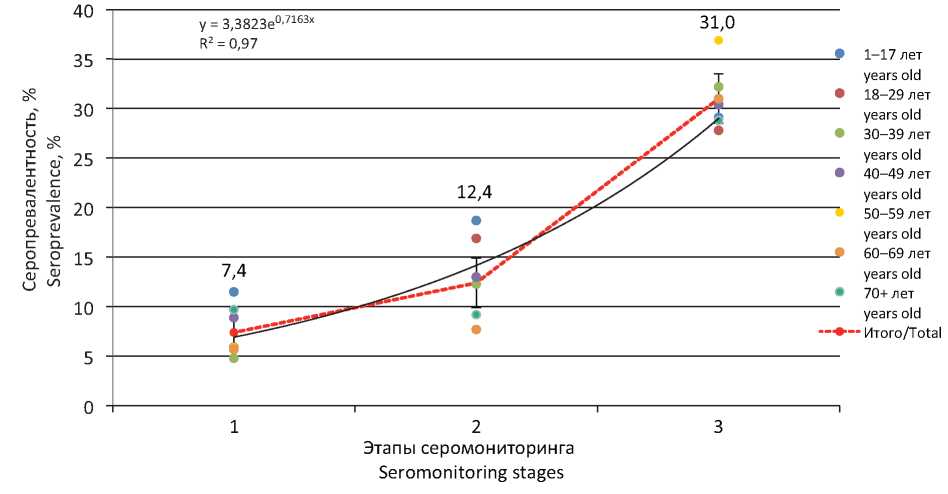
Результаты. Серопревалентность населения области составила 9,1% (95% ДИ 8,0–10,2): максимум у детей 14–17 лет (17,6%; 95% ДИ 12,3–23,9) и лиц в возрасте 75+ лет (14,8%; 95% ДИ 11,4–18,8), минимум – среди лиц в возрасте 30–39 лет (4,9%; 95% ДИ 3,0–8,0). Повышенные показатели отмечены у неработающих (15,4%; 95% ДИ 9,9–17,1) и прочих лиц (13,0%; 95% ДИ 8,6–18,5). Среди реконвалесцентов COVID-19 она была равной 33,3% (95% ДИ 16,3–59,0); у контактных лиц – 19,0% (95% ДИ 13,9–25,0). Более 94,7% (95% ДИ 91,2–97,2) серопозитивных лиц не имели манифестных проявлений. При серологическом мониторинге серопревалентность увеличивалась от 7,4% (95% ДИ 6,2–8,9) на 1-м этапе до 12,4% (95% ДИ 10,6–14,3) на 2-м и 31% (95% ДИ 28,8–33,3) – на 3-м этапах.
Заключение. Популяционный иммунитет к SARS-CoV-2 не достиг порогового уровня, что не исключает обострения эпидемического процесса.
Ключевые слова
Полный текст
Открыть статью на сайте журналаОб авторах
А. Ю. Попова
Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека (Роспотребнадзор)
ORCID iD: 0000-0003-2567-9032
127994, Москва, Россия
РоссияВ. С. Смирнов
ФБУН «Санкт-Петербургский научно-исследовательский институт эпидемиологии и микробиологии им. Пастера» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (Роспотребнадзор)
Автор, ответственный за переписку.
Email: vssmi@mail.ru
ORCID iD: 0000-0002-2723-1496
Смирнов Вячеслав Сергеевич, д-р мед. наук, профессор, ведущий научный сотрудник лаборатории молекулярной иммунологии
197101, Санкт-Петербург, Россия
РоссияЕ. Б. Ежлова
Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека (Роспотребнадзор)
ORCID iD: 0000-0002-8701-280X
127994, Москва, Россия
РоссияА. А. Мельникова
Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека (Роспотребнадзор)
ORCID iD: 0000-0002-5651-1331
127994, Москва, Россия
РоссияЛ. В. Самойлова
Управление Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (Роспотребнадзор) по Новосибирской области
ORCID iD: 0000-0003-4836-9010
630132, Новосибирск, Россия
РоссияЛ. В. Лялина
ФБУН «Санкт-Петербургский научно-исследовательский институт эпидемиологии и микробиологии им. Пастера» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (Роспотребнадзор)
ORCID iD: 0000-0001-9921-3505
197101, Санкт-Петербург, Россия
РоссияЕ. В. Семёнова
ФБУЗ «Центр гигиены и эпидемиологии в Новосибирской области»
ORCID iD: 0000-0002-7715-7036
630099, Новосибирск, Россия
РоссияМ. А. Гурский
ФБУЗ «Центр гигиены и эпидемиологии в Новосибирской области»
ORCID iD: 0000-0002-5951-0940
630099, Новосибирск, Россия
РоссияЕ. А. Аксёнова
Министерство здравоохранения Новосибирской области
ORCID iD: 0000-0001-6515-2169
630007, Новосибирск, Россия
РоссияТ. В. Арбузова
ФБУН «Санкт-Петербургский научно-исследовательский институт эпидемиологии и микробиологии им. Пастера» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (Роспотребнадзор)
ORCID iD: 0000-0002-3074-8656
197101, Санкт-Петербург, Россия
РоссияА. А. Тотолян
ФБУН «Санкт-Петербургский научно-исследовательский институт эпидемиологии и микробиологии им. Пастера» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (Роспотребнадзор)
ORCID iD: 0000-0003-4571-8799
197101, Санкт-Петербург, Россия
РоссияСписок литературы
- WHO. Disease outbreak news – China. Available at: https://www.who.int/ru/emergencies/disease-outbreak-news/item/2020-DON229 (accessed August 12, 2021).
- Novel Coronavirus(2019-nCoV). Situation Report - 10. Available at: https://www.who.int/docs/default-source/coronaviruse/situationreports/20200130-sitrep-10-ncov.pdf (accessed August 12, 2021).
- Holshue M.L., DeBolt C., Lindquist S, Lofy K.H., Wiesman J., Bruce H., et al. First case of 2019 novel coronavirus in the United States. N. Engl. J. Med. 2020; 382(10): 929–36. https://doi.org/10.1056/nejmoa2001191
- WHO. Director-General’s remarks at 2019-nCoV coronavirus infection press briefing, 11 February 2020. Available at: https://www.who.int/ru/dg/speeches/detail/who-director-general-s-remarks-atthe-media-briefing-on-2019-ncov-on-11-february-2020 (accessed August 12, 2021).
- Коронавирус. Онлайн карта распространения коронавируса. Коронавирус в России и мире. Available at: https://www.coronavirus-monitor.ru (accessed August 12, 2021).
- Tay M.Z., Poh C.M., Rénia L., MacAry P.A., Ng L.F.P. The trinity of COVID-19: immunity, inflammation and intervention. Nat. Rev. Immunol. 2020; 20(6): 363–74. https://doi.org/10.1038/s41577-020-0311-8
- Ni L., Ye F., Cheng M.L., Feng Y., Deng Y.Q., Zhao H., et al. Detection of SARS-CoV-2-specific humoral and cellular immunity in COVID-19 convalescent individuals. Immunity. 2020; 52(6): 971–7. https://doi.org/10.1016/j.immuni.2020.04.023
- Hou H., Wang T., Zhang B., Luo Y., Mao L., Wang F., et al. Detection of IgM and IgG antibodies in patients with coronavirus disease 2019. Clin. Transl. Immunology. 2020; 9(5): e01136. https://doi.org/10.1002/cti2.11363
- Deeks J.J., Dinnes J., Takwoingi Y., Davenport C., Spijker R., Taylor- Phillips S., et al. Cochrane COVID-19 diagnostic test accuracy group. Antibody tests for identification of current and past infection with SARS-CoV-2. Cochrane Database Syst. Rev. 2020; 6(6): CD013652. https://doi.org/10.1002/14651858.CD013652
- Randolph H.E., Barreiro L.B. Herd immunity: Understanding COVID-19. Immunity. 2020; 52(5): 737–41. https://doi.org/10.1016/j.immuni.2020.04.012
- Clemente-Suárez V.J., Hormeño-Holgado A., Jiménez M., Benitez- Agudelo J.C., Navarro-Jiménez E., Perez-Palencia N., et al. Dynamics of Population Immunity Due to the Herd Effect in the COVID-19 Pandemic. Vaccines (Basel). 2020; 8(2): E236. https://doi.org/10.3390/vaccines8020236
- Iyer A.S., Jones F.K., Nodoushani A., Kelly M., Becker M., Slater D., et al. Dynamics and significance of the antibody response to SARS-CoV-2 infection. medRxiv. 2020; 5(52): eabe0367. https://doi.org/10.1101/2020.07.18.20155374
- Попова А.Ю., Ежлова Е.Б., Мельникова А.А., Башкетова Н.С., Фридман Р.К., Лялина Л.В., и др. Популяционный иммунитет к вирусу SARS-CoV-2 среди населения Санкт-Петербурга в период эпидемии COVID-19. Проблемы особо опасных инфекций. 2020; (3): 124–30. https://doi.org/10.21055/0370-1069-2020-3-124-130
- Расчёт необходимой численности выборки. Available at: https://bstudy.net/672834/sotsiologiya/raschet_neobhodimoy_chislennosti_vyborki (accessed August 12, 2021).
- Simon A.K., Hollander G.A., McMichael A. Evolution of the immune system in humans from infancy to old age. Proc. Biol. Sci. 2015; 282(1821): 20143085. https://doi.org/10.1098/rspb.2014.3085
- Wald A., Wolfowitz J. Confidence limits for continuous distribution functions. Ann. Math. Stat. 1939; 10(2): 105–18.
- Agresti A., Coull B.A. Approximate Is Better than “Exact” for Interval Estimation of Binomial Proportions. Am. Stat. 1998; 52(2): 119–26. https://doi.org/10.2307/2685469
- Исследовательская компания «РАДАР». Калькулятор значимых различий (z-test). Available at: https://radar-research.ru/software/z-test_calculator/ (accessed August 12, 2021).
- Sanche S., Lin Y.T., Xu C., Romero-Severson E., Hengartner N., Ke R. High contagiousness and rapid spread of severe acute respiratory syndrome Coronavirus 2. Emerg. Infect. Dis. 2020; 26(7): 1470–7. https://doi.org/10.3201/eid2607.200282
- Lai C.C., Liu Y.H., Wang C.Y., Wang Y.H., Hsueh S.C., Yen M.Y., et al. Asymptomatic carrier state, acute respiratory disease, and pneumonia due to severe acute respiratory syndrome coronavirus 2 (SARS-CoV-2): Facts and myths. J. Microbiol. Immunol. Infect. 2020; 53(3): 404–12. https://doi.org/10.1016/j.jmii.2020.02.012
- Li R., Pei S., Chen B., Song Y., Zhang T., Yang W., Shaman J. Substantial undocumented infection facilitates the rapid dissemination of novel coronavirus (SARS-CoV-2). Science. 2020; 368(6490): 489–93. https://doi.org/10.1126/science.abb3221
- Long Q.X., Tang X.J., Shi Q.L., Li Q., Deng H.J., Yuan J., et al. Clinical and immunological assessment of asymptomatic SARSCoV-2 infections. Nat. Med. 2020; 26(8): 1200–4. https://doi.org/10.1038/s41591-020-0965-6
- Попова А.Ю., Ежлова Е.Б., Мельникова А.А., Смирнов В.С., Лялина Л.В., Козловских Д.Н. Особенности серопревалентности к SARS-CoV-2 населения Среднего и Южного Урала в ранний период пандемии COVID-19. Эпидемиология и Вакцинопрофилактика. 2021; 20(3): 8–18. https://doi.org/10.31631/2073-3046-2021-20-3-8-18
- Попова А.Ю., Андреева Е.Е., Бабура Е.А., Балахонов С.В., Башкетова Н.С., Буланов М.В., и др. Особенности формирования серопревалентности населения Российской Федерации к нуклеокапсиду SARS-CoV-2 в первую волну эпидемии COVID-19. Инфекция и иммунитет. 2021; 11(2): 297–323. https://doi.org/10.15789/2220-7619-FOD-1684
- Попова А.Ю., Ежлова Е.Б., Мельникова А.А., Балахонов С.В., Чеснокова М.В., Дубровина В.И., и др. Опыт исследования серопревалентности к вирусу SARS-CoV-2 населения Иркутской области в период вспышки COVID-19. Проблемы особо опасных инфекций. 2020; (3): 106–13. https://doi.org/10.21055/0370-1069-2020-3-106-113
- Borges L.P., Martins A.F., de Melo M.S., de Oliveira M.G.B., de Rezende Neto J.M., Dósea M.B., et al. Seroprevalence of SARSCoV-2 IgM and IgG antibodies in an asymptomatic population in Sergipe, Brazil. Rev. Panam. Salud. Publica. 2020; 44: e108. https://doi.org/10.26633/RPSP.2020.108
- Iyer A.S., Jones F.K., Nodoushani A., Kelly M., Becker M., Slater D., et al. Dynamics and significance of the antibody response to SARS-CoV-2 infection. medRxiv. 2020; 5(52): 20155374. https://doi.org/10.1101/2020.07.18.20155374
- Wu F., Wang A., Liu M., Wang Q., Chen J., Xia S., et al. Neutralizing antibody responses to SARS-CoV-2 in a COVID-19 recovered patient cohort and their implications. medRxiv. 2020; 20047365. https://doi.org/https://doi.org/10.1101/2020.03.30.20047365
- Lei Q., Li Y., Hou H.Y., Wang F., Ouyang Z.Q., Zhang Y., et al. Antibody dynamics to SARS-CoV-2 in asymptomatic COVID-19 infections. Allergy. 2021; 76(2): 551–61. https://doi.org/10.1111/all.14622
- Schaeffer B., Taylor B., Bushman M., Hanage W.P. The devil in the details: Herd immunity and pandemic response. Cell Host Microbe. 2021; 27(7): 1048. https://doi.org/10.1016/j.chom.2021.06.017
- Vabret N. Antibody responses to SARS-CoV-2 short-lived. Nat. Rev. Immunol. 2020; 20(9): 519. https://doi.org/10.1038/s41577-020-0405-3
Дополнительные файлы